Hỗ trợ tư vấn
Tư vấn - Giải đáp - Hỗ trợ đặt tài liệu
Mua gói Pro để tải file trên Download.vn (không bao gồm tài liệu cao cấp) và trải nghiệm website không quảng cáo
Tìm hiểu thêm »Giải bài tập KHTN 9 Bài 17: Dãy hoạt động hóa học của kim loại, một số phương pháp tách kim loại giúp các em học sinh nhanh chóng trả lời các câu hỏi thảo luận, luyện tập trong SGK Khoa học tự nhiên 9 Chân trời sáng tạo trang 77, 78, 79, 80.
Giải Khoa học tự nhiên 9 Bài 17 được biên soạn bám sát theo chương trình SGK. Đồng thời, cũng giúp thầy cô tham khảo để soạn giáo án Bài 17 - Chủ đề 6: Kim loại, sự khác nhau cơ bản giữa phi kim và kim loại cho học sinh của mình. Mời thầy cô và các em cùng theo dõi nội dung chi tiết trong bài viết dưới đây của Download.vn:
Kim loại sodium và magnesium phản ứng với nước có hiện tượng giống nhau không?
Trả lời:
Kim loại sodium và magnesium phản ứng với nước có hiện tượng không giống nhau.
+ Kim loại sodium phản ứng mạnh với nước ở ngay điều kiện thường.
+ Kim loại magnesium hầu như không phản ứng với nước ở điều kiện thường, phản ứng chậm với nước nóng và phản ứng mạnh với hơi nước nóng.
Nhận xét mức độ hoạt động hoá học của kim loại Na và Mg.
Trả lời:
Kim loại Na hoạt động hoá học mạnh hơn kim loại Mg.
Tiến hành Thí nghiệm 1 và nêu hiện tượng quan sát được. Viết phương trình hóa học của các phản ứng.
Trả lời:
- Học sinh tiến hành thí nghiệm theo các bước:
+ Bước 1: Cố định 3 ống nghiệm trên giá ống nghiệm, đánh số thứ tự 3 ống nghiệm.
+ Bước 2: Thêm vào lần lượt mỗi ống nghiệm 2 mL dung dịch HCl.
+ Bước 3: Cho vào ống nghiệm (1) một mảnh magnesium, ống nghiệm (2) một đinh sắt và ống nghiệm (3) một mảnh đồng phoi bào.
- Hiện tượng:
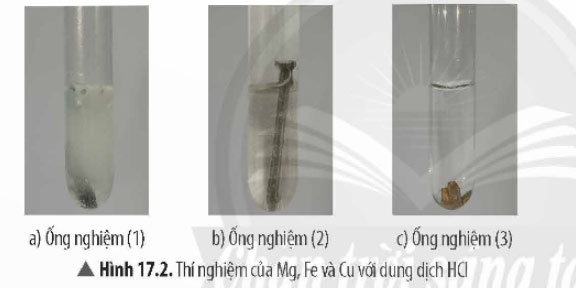
+ Ống nghiệm 1: Phản ứng xảy ra mãnh liệt. Mảnh Mg tan dần, có khí thoát ra mạnh.
+ Ống nghiệm 2: Có phản ứng xảy ra, phản ứng êm dịu hơn so với ở ống nghiệm 1. Đinh sắt tan dần, có khí thoát ra.
+ Ống nghiệm 3: Không có hiện tượng gì xuất hiện.
- Phương trình hoá học:
+ Ống nghiệm 1: Mg + 2HCl → MgCl2 + H2.
+ Ống nghiệm 2: Fe + 2HCl → FeCl2 + H2.
Nhận xét mức độ hoạt động hoá học của kim loại Fe, Cu, Mg.
Trả lời:
Mức độ hoạt động hoá học của các kim loại giảm dần theo thứ tự: Mg, Fe, Cu.
Tiến hành Thí nghiệm 2 và và nêu hiện tượng quan sát được. Viết phương trình hoá học của các phản ứng.
Trả lời:
- Học sinh tiến hành thí nghiệm theo các bước sau:
+ Cố định 2 ống nghiệm trên giá để ống nghiệm, đánh số thứ tự 2 ống nghiệm.
+ Cho vào ống nghiệm (1) 2mL dung dịch ZnSO4 và ống nghiệm (2) 2 mL dung dịch AgNO3.
+ Nhúng vào mỗi ống nghiệm một đoạn dây đồng, quan sát hiện tượng.

- Hiện tượng:
+ Ống nghiệm 1: Không có hiện tượng gì xuất hiện.
+ Ống nghiệm 2: Có lớp kim loại trắng sáng bám ngoài dây đồng; dung dịch chuyển từ không màu sang màu xanh.
- Phương trình hoá học:
Cu + ZnSO4 → không phản ứng
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Nhận xét mức độ hoạt động hoá học của kim loại Cu, Zn, Ag.
Trả lời:
+ Cu không phản ứng với ZnSO4 ⇒ Cu hoạt động hoá học kém hơn Zn.
+ Cu đẩy được Ag ra khỏi muối ⇒ Cu hoạt động hoá học mạnh hơn Ag.
Mức độ hoạt động hoá học của các kim loại giảm dần theo thứ tự: Zn, Cu, Ag.
Trong công nghiệp, phương pháp nào được sử dụng để sản xuất nhôm? Nguyên liệu để sản xuất nhôm là gì?
Trả lời:
- Trong công nghiệp, phương pháp điện phân nóng chảy được sử dụng để sản xuất nhôm.
- Nguyên liệu để sản xuất nhôm là quặng bauxite (thành phần chủ yếu là aluminium oxide).
Người ta đã dùng phương pháp nào để tách Zn từ zinc sulfide? Viết phương trình hoá học xảy ra.
Trả lời:
- Người ta dùng phương pháp nhiệt luyện để tách Zn từ zinc sulfide.
- Phương trình hóa học:
+ Nung nóng quặng sphalerite (thành phần chính là ZnS) ở nhiệt độ cao với luồng không khí trong lò để chuyển thành zinc oxide theo phương trình hóa học:
2ZnS + 3O2 ![]() \(\overset{to}{\rightarrow}\) 2ZnO + 2SO2
\(\overset{to}{\rightarrow}\) 2ZnO + 2SO2
+ Cho ZnO phản ứng với C ở nhiệt độ cao thu được kẽm (Zn):
ZnO + C ![]() \(\overset{to}{\rightarrow}\) Zn + CO
\(\overset{to}{\rightarrow}\) Zn + CO
Khí nào sinh ra khi kim loại phản ứng với dung dịch HCl? Nêu ví dụ minh hoạ và viết phương trình hoá học của phản ứng.
Trả lời:
Khí hydrogen sinh ra khi kim loại phản ứng với dung dịch HCl.
Ví dụ: Cho kim loại Zn phản ứng với dung dịch HCl sinh ra muối chloride và giải phóng khí hydrogen.
Phương trình hoá học:
Zn + 2HCl → ZnCl2 + H2
Hoàn thành phương trình hoá học của các phản ứng sau:
a) Ca + H2O →
b) Fe + HCl →
c) Zn + CuSO4 →
Trả lời:
a) Ca + 2H2O → Ca(OH)2 + H2;
b) Fe + 2HCl → FeCl2 + H2;
c) Zn + CuSO4 → ZnSO4 + Cu.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: