Hỗ trợ tư vấn
Tư vấn - Giải đáp - Hỗ trợ đặt tài liệu
Mua gói Pro để tải file trên Download.vn (không bao gồm tài liệu cao cấp) và trải nghiệm website không quảng cáo
Tìm hiểu thêm »Giải bài tập Khoa học tự nhiên 7 Bài 4: Sơ lược bảng tuần hoàn các nguyên tố hóa học hay nhất, ngắn gọn giúp các em học sinh dễ dàng làm bài tập trong SGK Khoa học tự nhiên 7 Chân trời sáng tạo trang 22, 23, 24, 25, 26, 27, 28, 29, 30.
Qua đó, giúp các em nắm được cấu tạo của bảng tuần hoàn các nguyên tố hóa học. Đồng thời, cũng giúp thầy cô tham khảo soạn giáo án Bài 4 Chủ đề 1: Nguyên tử - Nguyên tố hóa học - Sơ lược về bảng tuần hoàn các nguyên tố hóa học cho học sinh của mình. Vậy mời thầy cô và các em cùng theo dõi bài viết dưới đây của Download.vn:
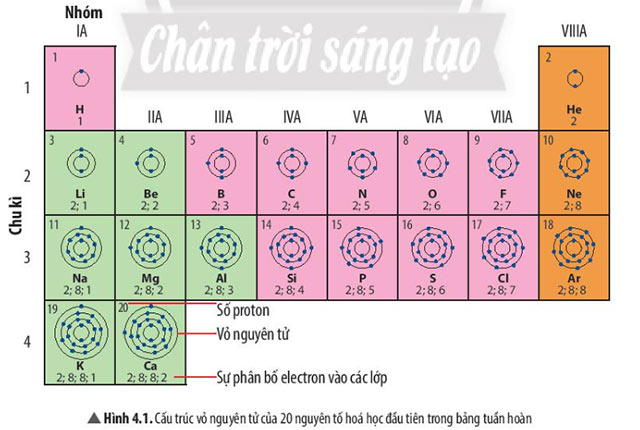
Quan sát Hình 4.1, em hãy cho biết:
a) Nguyên tử của những nguyên tố nào có cùng số lớp electron
b) Nguyên tử của những nguyên tố nào có số electron ở lớp ngoài cùng bằng nhau
Trả lời:
a) Những nguyên tố nằm ở cùng 1 chu kì có số lớp electron bằng nhau
- Ví dụ: Các nguyên tố ở chu kì 1 có 1 lớp electron, các nguyên tố ở chu kì 2 có 2 lớp electron, nguyên tố ở chu kì 3 có 3 lớp electron
b) Những nguyên tố nằm ở cùng 1 nhóm có số electron ở lớp ngoài cùng bằng nhau
- Ví dụ: Các nguyên tố nhóm IA có 1 electron ở lớp ngoài cùng, nguyên tố nhóm VIIA có 7 electron ở lớp ngoài cùng
- Trừ nguyên tố He nằm ở nhóm VIIIA nhưng có 2 electron ở lớp ngoài cùng
Dựa vào thông tin được cung cấp và Hình 4.2, em hãy cho biết bảng tuần hoàn được cấu tạo như thế nào?
Trả lời:
Bảng tuần hoàn gồm các nguyên tố hóa học mà vị trí được đặc trưng bởi ô nguyên tố, chu kì và nhóm
Các nguyên tố họ lanthanide và họ actinide được xếp riêng thành 2 hàng ở cuối bảng tuần hoàn
Số hiệu nguyên tử của một nguyên tố hóa học cho biết những thông tin gì về nguyên tố đó.
Trả lời:
- Số hiệu nguyên tử = số đơn vị điện tích hạt nhân = số proton trong hạt nhân = số electron trong nguyên tử = số thứ tự của nguyên tố trong bảng tuần hoàn
- Ví dụ: Nguyên tử hydrogen có số hiệu nguyên tử là 1
=> Nguyên tố hydrogen ở ô số 1 trong bảng tuần hoàn, điện tích hạt nhân là +1 (do có 1 proton trong hạt nhân) và có 1 electron trong nguyên tử
Quan sát Hình 4.4 và trả lời các câu hỏi sau:
a) Mỗi chu kì bắt đầu từ nhóm nào và kết thúc ở nhóm nào?
b) Em hãy chỉ ra sự tuần hoàn ở mỗi chu kì trong bảng tuần hoàn các nguyên tố hóa học.

Trả lời:
a) Mỗi chu kì bắt đầu từ nhóm IA và kết thúc ở nhóm VIIIA
b) Trong 1 chu kì, xét từ trái qua phải, số electron ở lớp ngoài cùng tăng dần từ 1 đến 8
Khi bắt đầu 1 chu kì mới, nguyên tố đầu tiên có 1 electron ở lớp ngoài cùng tương ứng với nhóm IA và tăng dần đến 8 tương ứng với nhóm VIIIA
Quan sát Hình 4.5, cho biết những nguyên tố nào có tính chất tương tự nhau

Trả lời:
- Các nguyên tố trong cùng 1 nhóm (cùng 1 cột dọc) sẽ có tính chất hóa học tương tự nhau
=> Các nguyên tố nhóm IA (trừ H) đều là nguyên tố kim loại hoạt động mạnh
Các nguyên tố nhóm VIIA đều là nguyên tố phi kim hoạt động mạnh
Các nguyên tố nhóm VIIIA đều là các khí hiếm, trơ, không tham gia các phản ứng
Dựa vào bảng tuần hoàn (Hình 4.2), em hãy cho biết vị trí (nhóm, chu kì) của các nguyên tố K, Mg, Al.
Trả lời:
- Nguyên tố K
- Nguyên tố Mg
- Nguyên tố Al
Một kim loại ở thể lỏng trong điều kiện thường, được ứng dụng để chế tạo nhiệt kế. Đó là kim loại nào? Cho biết vị trí (chu kì, nhóm) của nguyên tố kim loại đó.
Trả lời:
- Kim loại ở thể lỏng trong điều kiện thường, được ứng dụng để chế tạo nhiệt kế là: Mercury (thủy ngân) có kí hiệu hóa học là Hg
- Mercury nằm ở nhóm IIB, chu kì 6 (hàng số 6)
Carbon, nitrogen, oxygen và chlorine là những nguyên tố phi kim phổ biến và gần gũi trong đời sống. Em hãy cho biết vị trí (nhóm, chu kì) của chúng trong bảng tuần hoàn.
Sử dụng Hình 4.1, em hãy nhận xét về số electron lớp ngoài cùng trong nguyên tử của các nguyên tố khí hiếm.

Trả lời:
- Nguyên tố khí hiếm thuộc nhóm VIIIA trong bảng tuần hoàn
- Các nguyên tố thuộc nhóm VIIIA (trừ He) đều có 8 electron ở lớp ngoài cùng
=> Ngoài He có 2 electron ở lớp ngoài cùng thì các nguyên tố khí hiếm đều có 8 electron ở lớp ngoài cùng
Dựa vào cơ sở nào để xếp các nguyên tố hóa học trong bảng tuần hoàn.
Trả lời:
Cơ sở để xếp các nguyên tố hóa học trong bảng tuần hoàn là:
Cho biết những thông tin cơ bản về nguyên tố hóa học đã cho dưới đây:

Trả lời:
Cho biết:
Dựa vào Hình 4.2, hãy hoàn thành các thông tin còn thiếu trong bảng sau:
| Nguyên tố | Kí hiệu hóa học | Nhóm | Chu kì |
| Calcium | ? | ? | ? |
| ? | P | ? | ? |
| Xenon | ? | ? | ? |
Trả lời:
| Nguyên tố | Kí hiệu hóa học | Nhóm | Chu kì |
| Calcium | Ca | IIA | 4 |
| Phosphorus | P | VA | 3 |
| Xenon | Xe | VIIIA | 5 |
Mỗi kim loại đều có vai trò và ứng dụng khác nhau trong đời sống, em hãy cho biết những kim loại nào thường được sử dụng để làm trang sức. Dựa vào Hình 4.2, hãy cho biết vị trí (ô, chu kì, nhóm) của chúng trong bảng tuần hoàn.
Trả lời:
Những kim loại thường được sử dụng làm đồ trang sức: Vàng (gold), bạc (silver), platinum.
Tìm hiểu qua thực tế, hãy cho biết nguyên tố phi kim nào có trong thành phần của kem đánh răng. Nguyên tố phi kim nào có trong thành phần muối ăn? Chúng thuộc chu kì và nhóm nào trong bảng tuần hoàn.
Trả lời:
Trong kem đánh răng thường có muối của nguyên tố fluorine (F) có tác dụng bảo vệ lớp men răng giúp răng chắc khỏe.
Trong bảng tuần hoàn, các nguyên tố hóa học được sắp xếp theo
A. thứ tự chữ cái trong từ điển
B. thứ tự tăng dần điện tích hạt nhân
C. thứ tự tăng dần số hạt electron lớp ngoài cùng
D. thứ tự tăng dần số hạt neutron
Trả lời:
Các nguyên tố hóa học trong bảng tuần hoàn được sắp xếp theo chiều tăng dần điện tích hạt nhân của nguyên tử
=> Đáp án B
Những nguyên tố hóa học nào sau đây thuộc cùng một nhóm?
A. O, S, Se
B. N, O, F
C. Na, Mg, K
D. Ne, Na, Mg
Trả lời:
A: O, S, Se thuộc cùng nhóm VIA
B: N thuộc nhóm VA, O thuộc nhóm VIA, F thuộc nhóm VIIA
C: Na, K thuộc nhóm IA, Mg thuộc nhóm IIA
D: Ne thuộc nhóm VIIIA, Na thuộc nhóm IA, Mg thuộc nhóm IIA
=> Đáp án A
Những nguyên tố hóa học nào sau đây thuộc cùng một chu kì?
A. Li, Si, Ne
B. Mg, P, Ar
C. K, Fe, Ag
D. B, Al, In
Trả lời:
A: Li thuộc chu kì 2, Si thuộc chu kì 3, Ne thuộc chu kì 2
B: Mg, P, Ar đều thuộc chu kì 3
C: K, Fe thuộc chu kì 4, Ag thuộc chu kì 5
D: B thuộc chu kì 2, Al thuộc chu kì 3, In thuộc chu kì 5
=> Đáp án B
Cho các nguyên tố sau: Ge, S, Br, Pb, C, Mo, Ba, Ar, Hg. Hãy sắp xếp chúng vào bảng dưới đây.
|
Kim loại |
Phi kim |
Khí hiếm |
|
? |
? |
? |
Trả lời:
|
Kim loại |
Phi kim |
Khí hiếm |
|
Ge, Pb, Mo, Ba, Hg |
S, Br, C |
Ar |
Xác định vị trí (ô nguyên tố, chu kì, nhóm) của các nguyên tố sau trong bảng tuần hoàn
a) Magnesium (Mg)
b) Neon (Ne)
Trả lời:
a) Nguyên tố Magnesium (Mg)
b) Nguyên tố Neon (Ne)
Tìm hiểu từ internet hay tài liệu (sách, báo), em hãy viết một đoạn thông tin về nguyên tố hóa học cần thiết cho sự hô hấp của con người và sinh vật trên Trái Đất.
Trả lời:
Oxygen cần thiết cho sự sống
Oxygen cần thiết cho sự cháy và quá trình đốt cháy nhiên liệu
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: