Hỗ trợ tư vấn
Tư vấn - Giải đáp - Hỗ trợ đặt tài liệu
Mua gói Pro để tải file trên Download.vn và trải nghiệm website không quảng cáo
Tìm hiểu thêm »Giải Khoa học tự nhiên 8 Bài 5: Mol và tỉ khối của chất khí giúp các em học sinh lớp 8 trả lời các câu hỏi phần thảo luận, luyện tập trang 27, 28, 29, 30, 31 sách Chân trời sáng tạo.
Giải KHTN 8 Bài 5 Chân trời sáng tạo giúp các em học sinh hiểu được kiến thức về cách xác định tỉ khối của chất khí. Đồng thời là tư liệu hữu ích giúp thầy cô soạn giáo án cho riêng mình. Vậy sau đây là nội dung chi tiết bài giải KHTN 8 Bài 5 Mol và tỉ khối của chất khí mời các bạn cùng theo dõi và tải tại đây.
Tại sao ta không thể đếm được chính xác số nguyên tử hay phân tử của một chất?
Trả lời:
Do nguyên tử hay phân tử của một chất là vô cùng nhỏ nên việc đếm chính xác số nguyên tử hay phân tử trong một lượng chất gần như không thể thực hiện được.
Nếu xét cùng 1 mol thì khối lượng của C và Cu có giá trị là bao nhiêu gam?
Trả lời:
- Khối lượng của 1 mol C là 12 gam.
- Khối lượng của 1 mol Cu là 64 gam.
Nếu các chất có cùng số mol thì có cùng khối lượng không?
Trả lời:
Các chất có cùng số mol chưa chắc đã cùng khối lượng.
Ví dụ:
1 mol Cu có khối lượng 64 gam.
1 mol SO2 có khối lượng 64 gam.
1 mol H2 có khối lượng 2 gam.
So sánh trị số của khối lượng mol nguyên tử, khối lượng mol phân tử với khối lượng nguyên tử, khối lượng phân tử tương ứng của các chất đã cho trong Bảng 5.1.
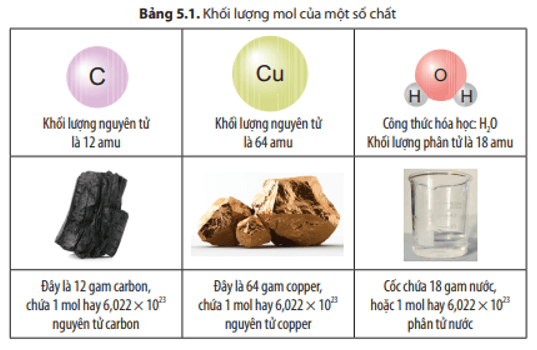
Trả lời:
Khối lượng mol nguyên tử hay khối lượng mol phân tử của một chất có cùng trị số với khối lượng nguyên tử hay khối lượng phân tử của chất đó.
Em có nhận xét gì về thể tích của 1 mol các chất khí ở cùng điều kiện về nhiệt độ và áp suất trong Hình 5.3.
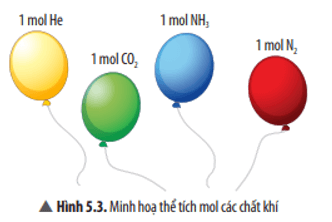
Trả lời:
Thể tích của 1 mol các chất khí ở cùng điều kiện về nhiệt độ và áp suất trong Hình 5.3 là bằng nhau.
Ở nhiệt độ 25oC và áp suất là 1 bar, 1 mol chất khí bất kì có thể tích bằng bao nhiêu lít?
Trả lời:
Ở nhiệt độ 25oC và áp suất là 1 bar, 1 mol chất khí bất kì có thể tích bằng 24,79 lít.
Làm thế nào để tính được thể tích các chất khí ở điều kiện chuẩn?
Trả lời:
Gọi n là số mol chất khí (mol); V là thể tích của chất khí ở đktc (lít), ta có công thức chuyển đổi sau: V = n × 24,79.
Bằng cách nào ta có thể biết được khí A nặng hay nhẹ hơn khí B?
Trả lời:
Để biết khí A nặng hay nhẹ hơn khí B bao nhiêu lần, ta so sánh khối lượng của hai thể tích khí bằng nhau ở cùng điều kiện nhiệt độ và áp suất.
Hãy cho biết khối lượng phân tử và khối lượng mol của các chất trong bảng sau
|
Chất |
Khối lượng nguyên tử (amu) |
Khối lượng phân tử (amu) |
Khối lượng (gam/ mol) |
|
Ethanol (C2H5OH) |
H = 1 C = 12 O = 16 |
? |
? |
|
Muối ăn (NaCl) |
Na = 23 Cl = 35,5 |
? |
? |
Trả lời:
|
Chất |
Khối lượng nguyên tử (amu) |
Khối lượng phân tử (amu) |
Khối lượng (gam/ mol) |
|
Ethanol (C2H5OH) |
H = 1 C = 12 O = 16 |
46 |
46 |
|
Muối ăn (NaCl) |
Na = 23 Cl = 35,5 |
58,5 |
58,5 |
a) Tính khối lượng của 0,5 mol phân tử bromine, biết rằng phân tử bromine có 2 nguyên tử và 1 mol nguyên tử bromine có khối lượng là 80 gam.
b) Tìm khối lượng mol của hợp chất A, biết rằng 0,5 mol của hợp chất này có khối lượng là 22 gam.
Trả lời:
a) Khối lượng mol phân tử bromine: MBr2=80×2 = 160 g/mol;
Khối lượng của 0,5 mol phân tử bromine:
mBr2=0,5×160 = 80 gam.
b) Khối lượng mol của hợp chất A:
a) Hãy cho biết 0,1 mol CO2 ở đktc có thể tích là bao nhiêu lít.
b) 4,958 lít khí O2 (đkc) có số mol là bao nhiêu?
Trả lời:
a) VCO2=0,1×24,79=2,479 (lit).
b) nO2 = ![]() \(\frac{4,958}{24,79}=0,2\) (mol).
\(\frac{4,958}{24,79}=0,2\) (mol).
Hãy cho biết khí oxygen nặng hay nhẹ hơn khí hydrogen bao nhiêu lần?
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: