Hỗ trợ tư vấn
Tư vấn - Giải đáp - Hỗ trợ đặt tài liệu
Mua gói Pro để tải file trên Download.vn (không bao gồm tài liệu cao cấp) và trải nghiệm website không quảng cáo
Tìm hiểu thêm »Giải Khoa học tự nhiên 8 Bài 7: Nồng độ dung dịch giúp các em học sinh lớp 8 trả lời các câu hỏi phần thảo luận, luyện tập trang 35, 36, 37, 38 sách Chân trời sáng tạo.
Giải KHTN 8 Bài 7 Chân trời sáng tạo giúp các em học sinh hiểu được kiến thức về cách tính nồng độ dung dịch của các chất. Đồng thời là tư liệu hữu ích giúp thầy cô soạn giáo án cho riêng mình. Vậy sau đây là nội dung chi tiết bài giải KHTN 8 Bài 7 Nồng độ dung dịch mời các bạn cùng theo dõi và tải tại đây.
Hãy xác định chất tan và dung môi trong các dung dịch tạo thành ở Hình 7.1.
Trả lời:
- Trong dung dịch muối: chất tan là muối ăn (NaCl); dung môi là nước.
- Trong dung dịch đường: chất tan là đường (C12H22O11); dung môi là nước.
Tại sao lại gọi nước đường, nước muối là các dung dịch?
Trả lời:
Khi hòa tan đường hay muối (chất rắn) vào nước (chất lỏng) sẽ tạo thành nước đường hay nước muối (hỗn hợp đồng nhất).
Do đó có thể gọi nước đường, nước muối là các dung dịch.
Độ tan của một chất trong nước phụ thuộc vào những yếu tố nào?
Trả lời:
Độ tan của một chất trong nước phụ thuộc vào nhiệt độ. Ngoài ra đối với chất khí, độ tan phụ thuộc vào nhiệt độ và áp suất.
Quan sát đồ thị Hình 7.2, hãy nhận xét độ tan của một số chất rắn và chất khí thay đổi như thế nào khi tăng nhiệt độ.
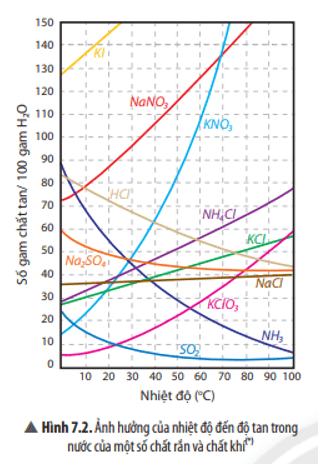
Trả lời:
- Độ tan của chất rắn sẽ tăng khi tăng nhiệt độ (trừ số ít trường hợp như Na2SO4 …)
- Độ tan của chất khí sẽ tăng khi giảm nhiệt độ.
Quan sát Hình 7.3, hãy cho biết vì sao 3 dung dịch của cùng một chất nhưng màu sắc của chúng lại khác nhau.

Trả lời:
3 dung dịch của cùng một chất nhưng màu sắc của chúng lại khác nhau do nồng độ của chúng khác nhau.
Để tính nồng độ phần trăm của dung dịch ta cần biết những thông tin gì?
Trả lời:
Công thức tính nồng độ phần trăm của dung dịch:
![]() \(C\%=\frac{mct}{mdd}\times100(\%)\)
\(C\%=\frac{mct}{mdd}\times100(\%)\)
Để tính nồng độ phần trăm của dung dịch ta cần biết những thông tin:
+ Khối lượng chất tan (mct);
+ Khối lượng dung dịch (mdd).
Làm thế nào để xác định được nồng độ mol của dung dịch?
Trả lời:
Công thức tính nồng độ mol của dung dịch:
![]() \(CM=\frac{n}{Vdd}\)
\(CM=\frac{n}{Vdd}\)
Như vậy để tính nồng độ mol của dung dịch cần biết: số mol chất tan và thể tích dung dịch.
Tính độ tan của muối Na2CO3 trong nước ở 25oC. Biết rằng ở nhiệt độ này khi hòa tan hết 76,75 gam Na2CO3 trong 250 gam nước thì được dung dịch bão hoà.
Trả lời:
Áp dụng công thức:
![]() \(S=\frac{mct}{mdm}\times100=\frac{76,75}{250}\times100=30,7(g/100gnước).\)
\(S=\frac{mct}{mdm}\times100=\frac{76,75}{250}\times100=30,7(g/100gnước).\)
Hoà tan 21 gam KNO3 vào 129 gam nước thu được dung dịch KNO3. Tính nồng độ phần trăm của dung dịch KNO3 thu được.
Trả lời:
Khối lượng dung dịch = khối lượng dung môi + khối lượng chất tan
= 129 + 21 = 150 gam.
Nồng độ phần trăm của dung dịch KNO3 thu được là:
![]() \(C\%=\frac{mct}{mdd}\times100(\%)=\frac{21}{150}\times100(\%)=14(\%).\)
\(C\%=\frac{mct}{mdd}\times100(\%)=\frac{21}{150}\times100(\%)=14(\%).\)
Hoà tan 16 gam CuSO4 khan vào nước thu được 200 ml dung dịch CuSO4. Tính nồng độ mol của dung dịch CuSO4.
Từ muối ăn NaCl, nước cất và các dụng cụ cần thiết. Hãy tính toán và nêu cách pha chế 100 mL dung dịch NaCl có nồng độ 1 M.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: