Hỗ trợ tư vấn
Tư vấn - Giải đáp - Hỗ trợ đặt tài liệu
Mua gói Pro để tải file trên Download.vn (không bao gồm tài liệu cao cấp) và trải nghiệm website không quảng cáo
Tìm hiểu thêm »Giải Hoá 11 Bài 19: Carboxylic acid là tài liệu vô cùng hữu ích, giúp các em học sinh lớp 11 có thêm nhiều gợi ý tham khảo, nhanh chóng trả lời toàn bộ câu hỏi trong sách Cánh diều trang 132, 133, 134, 135, 136, 137,138, 139.
Soạn Hóa 11 Cánh diều Bài 19 được trình bày khoa học, chi tiết giúp các em rèn kỹ năng giải Hóa, so sánh đáp án vô cùng thuận tiện. Đồng thời đây cũng là tài liệu giúp quý thầy cô tham khảo để soạn giáo án cho riêng mình. Vậy sau đây là giải Hóa 11 Carboxylic acid Cánh diều, mời các bạn cùng theo dõi tại đây.
Hợp chất X có công thức cấu tạo: (CH3)2CHCH2COOH. Tên của X là
A. 2 – methylpropanoic acid.
B. 2 – methylbutanoic acid.
C. 3 – methylbutanoic acid.
D. 3 – methylbutan – 1 – oic acid.
Gợi ý đáp án
Đáp án đúng là: C
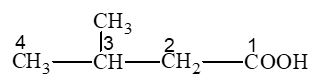
3 – methylbutanoic acid.
Chất nào sau đây có nhiệt độ sôi cao nhất?
A. Propan – 1 – ol.
B. Acetaldehyde.
C. Formic acid.
D. Acetic acid.
Gợi ý đáp án
Đáp án đúng là: D
Nhiệt độ sôi: Acetaldehyde < Propan – 1 – ol < Formic acid < Acetic acid.
Trình bày phương pháp hoá học để phân biệt các dung dịch sau: ethanol, glycerol, acetaldehyde và acetic acid.
Gợi ý đáp án
Trích mẫu thử.
Cho lần lượt từng mẫu quỳ tím vào từng mẫu thử:
- Quỳ tím chuyển sang màu đỏ → mẫu thử là acetic acid.
- Quỳ tím không đổi màu → mẫu thử là ethanol, glycerol, acetaldehyde (nhóm I).
Phân biệt nhóm I, dùng Cu(OH)2/OH-.
- Ở điều kiện thường:
+ Cu(OH)2 tan, sau phản ứng thu được dung dịch màu xanh đặc trưng → mẫu thử là glycerol.
+ Không có hiện tượng: ethanol, acetaldehyde (nhóm II).
- Tiếp tục đun nóng các ống nghiệm chứa thuốc thử Cu(OH)2/OH- và mẫu thử nhóm (II).
+ Xuất hiện kết tủa đỏ gạch → mẫu thử là acetaldehyde.
CH3CHO + 2Cu(OH)2 + NaOH ![]() \(\overset{t^{o} }{\rightarrow}\) CH3COONa + Cu2O (đỏ gạch) + 3H2O.
\(\overset{t^{o} }{\rightarrow}\) CH3COONa + Cu2O (đỏ gạch) + 3H2O.
+ Không hiện tượng → mẫu thử là ethanol.
Đun nóng 12 gam acetic acid với 13,8 gam ethanol (có dung dịch H2SO4 đặc làm xúc tác) thu được 11 gam ester. Tính hiệu suất của phản ứng ester hoá.
Gợi ý đáp án
nCH3COOH = ![]() \(\frac{12}{60}\) = 0,2(mol); nC2H5OH =
\(\frac{12}{60}\) = 0,2(mol); nC2H5OH = ![]() \(\frac{13,8}{46}\)6 = 0,3(mol)
\(\frac{13,8}{46}\)6 = 0,3(mol)
Phương trình hoá học:
CH3COOH + C2H5OH ![]() \(\overset{H_{2}SO_{4},t^{o} }{\rightleftharpoons}\) CH3COOC2H5 + H2O.
\(\overset{H_{2}SO_{4},t^{o} }{\rightleftharpoons}\) CH3COOC2H5 + H2O.
0,2 0,3 0,2 mol
Dựa vào PTHH có C2H5OH dư nên số mol ester sinh ra theo lí thuyết tính theo số mol CH3COOH.
Hiệu suất phản ứng ester hoá là:
H = ![]() \(\frac{m_{esterTT} }{m_{esterLT} }\) . 100% =
\(\frac{m_{esterTT} }{m_{esterLT} }\) . 100% = ![]() \(\frac{110,2}{88}\).100% = 62,5%.
\(\frac{110,2}{88}\).100% = 62,5%.
Giấm được sử dụng khá phổ biến để chế biến thức ăn. Bạn Mai muốn xác định nồng độ acetic acid có trong giấm ăn bằng cách sử dụng dung dịch sodium hydroxyde 0,1M để chuẩn độ. Bạn lấy mẫu giấm ăn đó để làm thí nghiệm và kết quả chuẩn độ 3 lần như bảng sau:
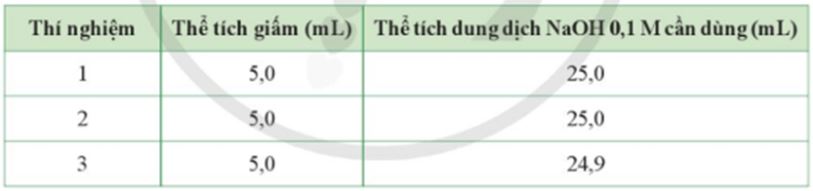
Hãy giúp bạn Mai xác định nồng độ mol của acetic acid trong giấm.
Gợi ý đáp án
Thể tích trung bình của dung dịch NaOH cần dùng:
VNaOH = ![]() \(\frac{25+25+24,9}{3}\) = 24,97(mL)
\(\frac{25+25+24,9}{3}\) = 24,97(mL)
Nồng độ acetic acid có trong giấm ăn là:
CM(CH3COOH) = ![]() \(\frac{24,97.0,1}{5}\) = 0,5M.
\(\frac{24,97.0,1}{5}\) = 0,5M.
Hợp chất X được dùng nhiều để tổng hợp polymer. Kết quả phân tích nguyên tố cho thấy X có %C = 50%, %H = 5,56% (về khối lượng), còn lại là O. Trên phổ đồ MS của X thấy xuất hiện peak của ion phân tử [M+] có giá trị m/z = 72. Trên phổ IR của X thấy xuất hiện một peak rộng từ 2 500 – 3 200 cm-1, một peak ở 1 707 cm-1. Lập luận và dự đoán công thức cấu tạo của X.
Gợi ý đáp án
%O = 100% - 50% - 5,56% = 44,44%.
Đặt công thức chung của X là: CxHyOz, ta có:
![]()
= 4,167 : 5,56 : 2,778 = 3 : 4 : 2.
Vậy công thức đơn giản nhất của X là C3H4O2.
Công thức phân tử của X có dạng: (C3H4O2)n.
Peak của ion phân tử [M+] có giá trị m/z = 72 nên phân tử khối của X là 72.
⇒ 72n = 72 ⇒ n = 1.
Trên phổ IR của X thấy xuất hiện một peak rộng từ 2 500 – 3 200 cm-1, một peak ở 1 707 cm-1 nên X là carboxylic acid. Công thức cấu tạo của X là:
CH2 = CH – COOH.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: