Hoá học 9 Bài 5: Luyện tập Tính chất hóa học của oxit và axit Giải Hoá học lớp 9 trang 21
Giải Hóa học 9 Bài 5 giúp các bạn học sinh có thêm nhiều gợi ý tham khảo để trả lời các câu hỏi phần nội dung bài học và câu hỏi cuối bài Luyện tập Tính chất hóa học của oxit và axit thuộc chương 1 Các loại hợp chất vô cơ.
Soạn Hóa 9 bài 5 Luyện tập Tính chất hóa học của oxit và axit được biên soạn với các lời giải chi tiết, đầy đủ và chính xác bám sát chương trình sách giáo khoa. Hi vọng đây sẽ là tài liệu cực kì hữu ích hỗ trợ các em học sinh lớp 9 trong quá trình giải bài tập. Ngoài ra các bạn xem thêm nhiều tài liệu khác tại chuyên mục Hóa học 9.
Hoá 9 Bài 5: Luyện tập Tính chất hóa học của oxit và axit
Lý thuyết Hóa học 9 Bài 5
I. Tính chất hóa học của oxit
1. Oxit bazơ : Oxit bazơ có những tính chất hóa học nào ?
a) Tác dụng với nước: Một số oxit bazơ tác dụng với nước tạo thành dung dịch bazơ (kiềm).
Thí dụ:
Na2O + H2O → 2NaOH
BaO + H2O → Ba(OH)2
Những oxit bazơ tác dụng với nước và do đó cũng tan được trong nước là: Na2O, K2O, CaO, BaO, Li2O, Rb2O, Cs2O, SrO.
b) Tác dụng với axit: Oxit bazơ + axit → muối + nước
Thí dụ:
BaO + 2HCl → BaCl2 + H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
c) Tác dụng với oxit axit: Một số oxit bazơ, là những oxit bazơ tan trong nước tác dụng với oxit axit tạo thành muối.
Thí dụ:
CaO + CO2 → CaCO3
2. Oxit axit: oxit axit có những tính chất hóa học nào ?
a) Tác dụng với nước: Nhiều oxit axit tác dụng với nước tạo thành dung dịch axit.
Thí dụ:
SO3 + H2O → H2SO4
P2O5 + 3H2O → 2H3PO4
Những oxit axit tác dụng được với nước và do đó cũng tan trong nước.
b) Tác dụng với dung dịch bazơ: Oxit axit + dd bazơ → muối + nước.
Thí dụ:
CO2 + Ca(OH)2 → H2O + CaCO3
Những oxit khác như SO2, P2O5,…. Cũng có phản ứng tương tự.
c) Tác dụng với oxit bazơ: Oxit axit tác dụng với một số oxit bazơ (tan) tạo thành muối.
Thí dụ:
CO2 + BaO → BaCO3
3. Oxit lưỡng tính : Một số oxit vừa tác dụng dung dịch axit, vừa tác dụng với dung dịch bazơ, gọi là oxit lưỡng tính.
Thí dụ như: Al2O3, ZnO, SnO, Cr2O3,…
Thí dụ:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
Al2O3 + 2NaOH → H2O + 2NaAlO2 (natri aluminat)
4. Oxit trung tính (hay là oxit không tạo muối): Một số oxit không tác dụng với axit, dung dịch, bazơ, nước, gọi là oxit trung tính như: NO, N2O, CO,…
Giải bài tập Hóa 9 Bài 5 trang 21
Câu 1
Có những oxit sau: SO2, CuO, CaO, Na2O, CO2. Hãy cho biết những oxit nào tác dụng được với.
a) Nước
b) Axit clohiđric
c) Natri hiđroxit
Viết các phương trình hóa học.
Gợi ý đáp án:
a) Oxit tác dụng với nước là:
SO2 + H2O → H2SO3
Na2O + H2O → 2NaOH
CO2 + H2O → H2CO3
b) Oxit tác dụng với HCl là:
CuO + 2HCl → CuCl2 + H2O
Na2O + 2HCl → 2NaCl + H2O
CaO + 2HCl → CaCl2 + H2O
c) Những oxit tác dụng với natri hiđroxit là:
SO2 + 2NaOH → Na2SO3 + H2O
CO2 + 2NaOH → Na2CO3 + H2O
Câu 2
Những oxit nào dưới đây có thể điều chế bằng:
a) Phản ứng hóa hợp? Viết phương trình hóa học.
b) Phản ứng hóa hợp và phản ứng phân hủy? Viết phương trình hóa học.
1) H2O.
2) CuO.
3) Na2O.
4) CO2.
5) P2O5.
c) Các oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2, Na2O, H2O
Gợi ý đáp án:
a) Cả 5 oxit đã cho có thể điều chế bằng phản ứng hóa hợp. Viết các phương trình hóa học
2H2 + O2 ![]() 2H2O
2H2O
2Cu + O2 ![]() 2CuO
2CuO
4Na + O2 ![]() 2Na2O
2Na2O
4P + 5O2 ![]()
![]() 2P2O5
2P2O5
C + O2 ![]() CO2
CO2
b) Các oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2.
Cu(OH)2 ![]() CuO + H2O
CuO + H2O
2Cu + O2 ![]() 2CuO
2CuO
CaCO3 ![]() CaO + CO2
CaO + CO2
2Ca + O2 ![]() 2CaO
2CaO
c) Các oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2, Na2O, H2O
2NaNO2 ![]() Na2O + N2 + ½ O2
Na2O + N2 + ½ O2
4Na + O2 ![]() 2Na2O
2Na2O
Ca(HCO3)2 ![]() CaCO3 + CO2 + H2O
CaCO3 + CO2 + H2O
2H2 + O2 ![]() 2H2O
2H2O
Câu 3
Khí CO được dùng làm chất đốt trong công nghiệp, có lẫn tạp chất là các khí CO2 và SO2. Làm thế nào có thể loại bỏ những tạp chất ra khỏi CO bằng hóa chất rẻ tiền nhất? Viết các phương trình hóa học xảy ra.
Gợi ý đáp án:
Cho hỗn hợp khí CO, CO2, SO2 lội từ từ qua dung dịch Ca(OH)2. CO2 và SO2 tác dụng với dung dịch Ca(OH)2 (dư) tạo chất không tan CaCO3 và CaSO3 còn lại khí CO không tác dụng thoát ra.
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O.
Câu 4
Cần phải điều chế một lượng muối đồng sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric:
a) Axit sunfuric tác dựng với đồng (II) oxit.
b) Axit sunfuric đặc tác dụng với kim loại đồng.
Giải thích cho câu trả lời.
Gợi ý đáp án:
a) H2SO4 + CuO → CuSO4 + H2O (1)
b) Cu + 2H2SO4(đặc) → CuSO4 + SO2 ↑ + 2H2O (2)
Giả sử cần điều chế a mol CuSO4
Theo pt(1) nH2SO4 = nCuSO4 = a mol
Theo pt (2) nH2SO4 = 2.nCuSO4 = 2a mol
Do đó để tiết kiệm ta nên theo phản ứng (1) (phương pháp a) thì lượng axit H2SO4 sử dụng ít hơn ở phản ứng (2).
Câu 5
Hãy thực hiện những chuyển đổi hóa học sau bằng cách viết những phương trình phản ứng hóa học (ghi điều kiện của phản ứng, nếu có).
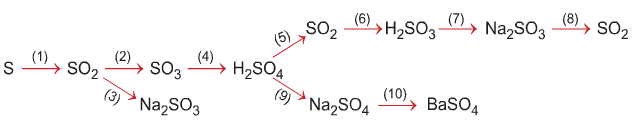
Gợi ý đáp án
Những chuyển đổi hóa học sau bằng cách viết những phương trình phản ứng hóa học (ghi điều kiện của phản ứng, nếu có).
1) S + O2 ![]() SO2
SO2
2) 2 SO2 + O2 ![]() 2 SO3
2 SO3
3) SO2 + Na2 O → Na2SO3
4) SO3 + H2O → H2SO4
5) 2H2SO4 (đ) + Cu ![]() CuSO4 + SO2↑ + 2 H2O
CuSO4 + SO2↑ + 2 H2O
6) SO2 + H2O → H2SO3
7) H2SO3 + 2 NaOH → Na2SO3 + 2H2O
8) Na2SO3 + 2HCl → 2 NaCl + SO2 ↑ + H2O
9) H2SO4 + 2 NaOH → Na2SO4 + 2H2O
10) Na2SO4 + BaCl2 → BaSO4 ↓ + 2 NaCl
- Lượt tải: 32
- Lượt xem: 926
- Dung lượng: 199,5 KB









 Hoá 9
Hoá 9