Hỗ trợ tư vấn
Tư vấn - Giải đáp - Hỗ trợ đặt tài liệu
Mua gói Pro để tải file trên Download.vn (không bao gồm tài liệu cao cấp) và trải nghiệm website không quảng cáo
Tìm hiểu thêm »
SỞ GIÁO DỤC VÀ ĐÀO TẠO
|
ĐỀ THI CHỌN HỌC SINH GIỎI CẤP TỈNH
|
Bài 1.
Chứng minh rằng tổng bình phương của 5 số nguyên liên tiếp không là số chính phương.
Bài 2.
Giải phương trình và hệ phương trình sau: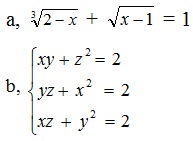
Bài 3.
Cho ABC có 3 góc đều nhọn. Gọi O là tâm đường tròn ngoại tiếp ABC; R, r theo thứ tự là độ dài bán kính đường tròn ngoại tiếp và đường tròn nội tiếp ABC; M, N, P lần lượt là hình chiếu vuông góc của O trên AB, BC và AC.
a, Chứng minh: BN.OM + BM.ON = BO.MN
b, Đặt ON = d1; OM = d2; OP = d3. Tính R + r theo d1, d2, d3?
Bài 4.
Lấy một số tự nhiên có 2 chữ số chia cho số có 2 chữ số viết theo thứ tự ngược lại thì được thương là 4 và dư 15. Nếu lấy số đó trừ đi 9 thì được một số bằng tổng bình phương của 2 chữ số tạo thành số đó. Tìm số tự nhiên ấy?
Câu 1: (4,5 điểm)
1. Khi cho dung dịch H3PO4 tác dụng với dung dịch NaOH tạo được dung dịch M.
a) Hỏi M có thể chứa những muối nào?
b) Phản ứng nào có thể xảy ra khi thêm KOH vào dung dịch M
c) Phản ứng nào có thể xảy ra khi thêm H3PO4 (hoặc P2O5) vào dung dịch M?
Viết phương trình húa học (PTHH) của cỏc phản ứng.
2. Hãy nêu một muối vừa tác dụng với HCl, vừa tác dụng với NaOH, thoả món điều kiện:
a) Cả hai phản ứng đều có khí thoát ra.
b) Phản ứng với HCl có khí bay lên và phản ứng với NaOH có kết tủa.
c) Cả hai phản ứng đều tạo kết tủa.
Câ 2: (4,0 điểm)
1. Cho các bình đựng các oxit riêng không nhãn sau: MgO, Na2O, P2O5 và ZnO dùng phương pháp hóa học hãy phân biệt các bình trên (chỉ dùng hai hoá chất khác), viết PTHH của các phản ứng để minh họa.
2. Hoàn thành các PTHH sau (ghi rõ điều kiện phản ứng nếu có):
a) FeS2 + O2 →
b) Fe3O4 + HCl →
c) Al2O3 + NaHSO4 →
d) Fe2O3 + CO → FexOy + CO2
Câ 3: (3,0 điểm)
1. Trộn V1 lít dung dịch HCl 1M với V2 lít dung dịch NaOH 2M được dung dịch X. Dung dịch X hoà tan được tối đa a mol Al(OH)3. Tìm biểu thức liên hệ giữa V1, V2 và a?
2. Cho ba bình mất nhãn:
- Bình X chứa dung dịch NaHCO3 và Na2CO3.
- Bình Y chứa dung dịch NaHCO3 và Na2SO4.
- Bình Z chứa dung dịch Na2CO3 và Na2SO4.
Chỉ dựng quỳ tím, dung dịch HCl, dung dịch Ba(OH)2 và ống nghiệm; hãy phân các bình trên? Viết PTHH của các phản ứng để minh hoạ.
Câ 4: (4,0 điểm)
Có 2 kim loại R và M, mỗi kim loại chỉ có một hoá trị. Cho dòng khí CO dư đi qua ống sứ nung nóng chứa hỗn hợp A gồm 2 oxit của 2 kim loại trên đến khi phản ứng hoàn toàn thì còn lại chất rắn A1 trong ống và khí A2 đi ra khỏi ống.
Dẫn khí A2 vào cốc đựng dung dịch Ba(OH)2 dư thu được 2,955g kết tủa.
Cho A1 tác dụng với dung dịch H2SO4 10% vừa đủ thì không có khí thoát ra, còn lại 0,96g chất rắn không tan và tạo ra dung dịch A3 có nồng độ 11,243%.
a) Xác định các kim loại R, M và công thức các oxit đã dùng.
b) Xác định thành phần phần trăm theo khối lượng của mỗi chất trong hỗn hợp A nếu biết rằng khi hoà tan hết A vào dung dịch HCl thì nồng độ phần trăm của hai muối trong dung dịch là bằng nhau.
Câu 5: (3,5 điểm)
Cho 6,8 gam hỗn hợp bột A gồm Fe và Mg vào 400 ml dung dịch CuSO4 nồng độ x mol/lít. Sau phản ứng thu được 9,2 gam chất rắn B và dung dịch C. Thêm NaOH dư vào dung dịch C được kết tủa. Nung kết tủa này ngoài không khí đến khối lượng không đổi thu được 6,0 gam chất rắn D. Tính thành phần phần trăm khối lượng mỗi kim loại trong A và tính x.
(Biết: H = 1, O = 16, C = 12,Cl = 35,5, Mg = 24, Fe = 56, Zn = 65, Ca = 40)
Câu 1 (8,0 điểm)
Có người cho rằng “Đời người dài dằng dặc, lãng phí một chút thời gian cũng chẳng có vấn đề gì”.
Suy nghĩ của em về quan niệm trên.
Câu 2 (12,0 điểm)
“Thơ văn hiện đại Việt Nam giai đoạn 1945 - 1975, ngoài hình ảnh người chiến sĩ trong sự nghiệp bảo vệ Tổ quốc còn mang nhịp thở của con người lao động mới”.
Bằng những hiểu biết về văn học giai đoạn này, em hãy làm sáng tỏ nhận định trên.
Download tài liệu để xem chi tiết.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: